Casi Clinici [DIABETE] Diabete mellito tipo 2 in stato catabolico acuto alla diagnosi (2010) |  |
AB è un uomo di 79 anni, altezza 173 cm, peso 99,5 kg, indice di massa corporea (body mass index [BMI]) 33,2 kg/m2, vedevo, pensionato.
Nell’agosto del 2006 giunge in accesso diretto c/o il nostro Servizio di Diabetologia e Malattie Metaboliche (SD) inviato dal DEA del nostro nosocomio per riscontro di iperglicemia marcata (563 mg/dl).
AB risiede per circa 6 mesi all’anno in abitazione isolata in montagna. Negli ultimi mesi sintomatologia caratterizzata da poliuria, polidipsia e calo ponderale (circa 7 kg), associata a balanopostite.
Non si è recato dal medico di medicina generale (MMG) se non recentemente. Il MMG ha prontamente prescritto terapia antimicotica per os e, nel sospetto di iperglicemia, ha inviato il suo assistito in DEA per gli accertamenti e le cure del caso.
In DEA AB è stato sottoposto a idratazione e.v. e infusione insulinica breve fino all’invio al nostro SD.
Nel nostro SD è attivo un Profilo di cura per i nuovi accessi, tra cui anche i casi di nuovo esordio clinico, secondo criteri di priorità clinica previsti dalla normativa regionale (DGR 14-10073 BU n. 38 del 18/05/2003); il protocollo clinico-organizzativo prevede la registrazione informatica di parametri bio-antropometrici e clinici su supporto informatico che permette l’estrazione di indicatori di processo e di esito intermedio.
Altri esami ematici a disposizione evidenziavano un valore di creatinina di 1,3 mg/dl, GFR (secondo la formula di Cockroft-Gault normalizzato per la superficie corporea) 41 ml/min/1,73 mq, modesta iponatriemia (128 mEq/l), emocromo e transaminasi in norma.
Alla raccolta anamnestica AB riferiva ricovero nel 1999 per infarto miocardico acuto (IMA) e ipertensione arteriosa; non altre patologie degne di nota. Riferiva inoltre un fratello affetto da diabete mellito. Riferiva come terapia domiciliare cardioASA, beta-bloccante, ACE-inibitore e furosemide.
Durante la prima visita di accoglienza (T0) è stata proposta e motivata la scelta di terapia insulinica intensiva (analogo rapido ai pasti + lento serale) ed ottenuto il consenso del paziente. AB è stato addestrato dall’infermiere professionale alla gestione della terapia (somministrazione dell’insulina, misurazione della glicemia e gestione dell’ipoglicemia) e giudicato “idoneo”. Dopo valutazione dietistica con consegna e spiegazione dello schema alimentare appropriato al fabbisogno energetico, AB è stato dimesso al domicilio dal SD con attestato di patologia e piano di automonitoraggio glicemico (PAG).
Obbiettivi
-
Efficace e rapido recupero dell’equilibrio glicemico e stabilizzazione del compenso nel medio-lungo termine
-
Coinvolgimento attivo del paziente nel percorso di cura (patient empowerment)
-
Adozione di un protocollo diagnostico-terapeutico condiviso da tutti i soggetti interessati (diabetologo, medico di medicina generale, infermieri, dietisti, paziente)
Domanda
Perché si è optato per una terapia insulinica intensiva?
Risposta
La Consensus dell’American Diabetes Association (ADA)/European Association for the Study of Diabetes (EASD) 2006 1 per la terapia dell’iperglicemia nel DMT2 prevede la terapia insulinica nello stato catabolico.
Nel DMT2 di nuova diagnosi con elevata glicemia a digiuno, un trattamento insulinico intensivo breve migliora la glucotossicità e il compenso glicemico a lungo termine 2-4.
Domanda
Poteva essere valutata una terapia farmacologia alternativa a quella insulinica o anche solo una modifica dello stile di vita?
Risposta
lo stato catabolico, caratterizzato da marcata iperglicemia, glucotossicità e sintomatologia da scompenso glicemico acuto aumenta il rischio di malattie sovrapposte con meccanismo “proinfettivo” e anche pro-trombotico e il solo intervento sullo stile di vita non è in grado di ripristinare l’omeostasi glicemica per lo meno in tempi relativamente rapidi.
L’iperglicemia costituisce l’alterazione metabolica specifica del diabete mellito ed è Il principale obiettivo del trattamento. Infatti, la nuova sfida nella terapia del diabete è contrastare la “memoria metabolica” 5, ovvero l’ambiente glicemico nella fase iniziale viene tenuto a memoria dall’organismo con persistenza negli organi, in particolare nell’endotelio, del danno indotto dall’iperglicemia mediante aumento dello stress ossidativo, principale meccanismo fisiopatologico delle complicanze. Questo dato è supportato da numerose evidenze e confermato da nuovi studi come l’ADVANCE (Action in Diabetes and Vascular Disease: preterAx and diamicroN-MR Controlled Evaluation) 6, che ha dimostrato che un compenso glicemico rigido del diabete mellito tipo 2 riduce il rischio di sviluppare l’endpoint composito di eventi micro- e macroangiopatici, e dai risultati del follow-up a lungo termine dell’UKPDS 7 che hanno dimostrato la persistenza negli anni dell’effetto benefico sulle complicanze vascolari di un trattamento intensivo della glicemia iniziato precocemente, cioè dal momento della diagnosi di diabete.
Come già detto, la Consensus dell’ADA/EASD 2006 1 per la terapia dell’iperglicemia nel DMT2 prevede la terapia insulinica nello stato catabolico. Studi precedenti 8 9 avevano sperimentato le sulfaniluree a dosaggio massimo in pazienti con diabete mellito scompensato (glicemia > 400 mg/dl) e avevano dimostrato di poter raggiungere il goal glicemico in un intervallo temporale relativamente breve (dimezzamento della glicemia a digiuno dopo 1 settimana e ulteriore dimezzamento dopo 4 mesi).
Peraltro, l’obiettivo della terapia diabetologica non deve essere unicamente focalizzata a normalizzare i livelli glicemici ma a preservare la funzione beta-cellulare residua in modo da procrastinare nel tempo il fenomeno del fallimento secondario. Infatti, l’iperglicemia persistente rappresenta, come noto, il meccanismo fisiopatologico della glucotossicità sulle beta-cellule pancreatiche. A tal proposito è stato condotto un ampio studio clinico controllato, l’ADOPT 10, che metteva a confronto sulfaniluree (glibenclamide), metformina e glitazone (rosiglitazone) in pazienti mai trattai prima con farmaci. Dopo 4 anni il fallimento della monoterapia si osservava nel 34% dei pazienti trattati con glibenclamide, nel 21% di quelli che assumevano metformina e solo nel 15% di quelli che utilizzavano rosiglitazone, mettendo in evidenza quindi che la “durability”, cioè la capacità di mantenere nel tempo l’efficacia ipoglicemizzante senza necessità di terapie aggiuntive, era minore per la sulfanilurea. La “durability” è secondaria alla preservazione della funzione secretoria beta-cellulare che si può ottenere con farmaci insulino-sensibilizzanti dopo un breve trattamento con terapia insulinica in caso di diabete mellito tipo 2 in stato catabolico alla diagnosi.
2° step
AB è stato pertanto dimesso dal nostro SD dopo addestramento alla gestione della terapia insulinica e all’automonitoraggio glicemico (consegnato il fabbisogno insulinico per iniziare il trattamento prescritto e il reflettometro). Sono state programmate successive rivalutazioni ambulatoriali a 3 (al primo controllo è prevista la verifica infermieristica dell’autosomministrazione insulinica e dell’autocontrollo glicemico), 8, 15 e 30 giorni e secondo necessità, in base alla remissione dei sintomi e ai valori della misurazione della glicemia per confronto con gli obiettivi definiti, personalizzati per età anagrafica (pre-pasti 90-140/150, dopo < 180/200). Sono stati richiesti esami di screening delle complicanze (fundus oculi, ECG, microalbuminuria).
Al primo controllo programmato il personale infermieristico ha dato parere positivo alla verifica dell’autosomministrazione insulinica e dell’automonitoraggio glicemico; è stato rispiegato il protocollo di correzione dell’ipoglicemia perché AB non aveva con sé le zollette di zucchero. È stata rivista con AB la necessità di una terapia alimentare con quantità costanti di carboidrati per ogni pasto (pesare gli alimenti che contengono glucidi). La terapia insulinica è stata confermata al dosaggio prescritto in precedenza.
AI successivi controlli ambulatoriali sono stati adeguati i dosaggi insulinici in base ai valori glicemici capillari rilevati da AB, fino al ripristino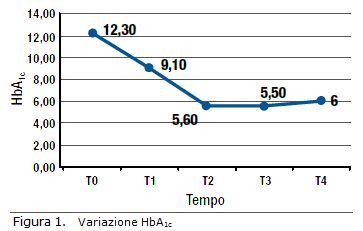 dell’omeostasi glicemica (valori glicemici negli obiettivi suddetti nella maggior parte delle determinazioni degli ultimi 10 giorni).
dell’omeostasi glicemica (valori glicemici negli obiettivi suddetti nella maggior parte delle determinazioni degli ultimi 10 giorni).
La terapia insulinica pertanto è stata sospesa dopo circa 4 settimane dall’inizio del trattamento (T1). Al T1 sono stati ripetuti gli esami ematochimici di routine con glicemia a digiuno di 109 mg/dl, HbA1c migliorata di 3 punti percentuali (9,1%), normalizzazione di creatinina e normalizzazione del GFR 66 ml/ min/1,73 mq e della natriemia. AB ha anche eseguito ECG e valutazione cardiologica che rilevava un buon compenso emodinamico in cardiopatia ischemica nota e stabilizzata. Al T1 in base agli esiti degli esami suddetti e ai valori dell’autocontrollo glicemico è stata sospesa la terapia insulinica e impostata la terapia ipoglicemizzante orale con insulino-sensibilizzante, metformina, iniziando con un dosaggio di 500 mg b.i.d. a colazione e cena. È stato peraltro confermata la prosecuzione, temporanea, dell’autocontrollo glicemico (PAG prescritto in deroga al T0 per 3 mesi per scompenso glicemico).
Dopo circa 20 giorni dallo switch terapeutico, ci contattava il MMG per comunicare valori glicemici capillari: in alcune misurazioni pre-pranzo e cena erano presenti valori tra 70 e 80, legati anche alla ripresa di una attività fisica più intensa (agricoltura e taglio della legna). Per tale motivo veniva consigliata la sospensione della metformina di colazione. Al successivo controllo ambulatoriale già programmato a un mese dalla sospensione insulinica si rilevavano valori glicemici a digiuno frequentemente vicino a 80; per questo AB si era autosospeso la metformina di cena. Si confermava pertanto la sola terapia alimentare e si sospendeva l’automonitoraggio glicemico domiciliare, consigliando ad AB il controllo del peso corporeo settimanale e di proseguire una alimentazione corretta e un’attività fisica regolare e con l’indicazione di contattarci in caso di malattie intercorrenti.
Al controllo programmato ai 6 mesi dalla diagnosi (T2) sono stati nuovamente ripetuti gli esami ematochimici di routine con glicemia a digiuno di 98 mg/dl, HbA1c ulteriormente migliorata (5,6%), creatinina 0,6 mg/dl, GFR 89 ml/min, microalbuminuria in norma, lipidi a target (colesterolo-LDL < 100, trigliceridi < 150 mg/dl) e transaminasi in norma; peso corporeo ridotto di 10 kg rispetto alla diagnosi. Al fundus oculi non segni di retinopatia diabetica e quadro compatibile con l’età anagrafica. AB riferisce benessere soggettivo. Viene confermata la sola terapia alimentare.
Domanda
Si è osservata un’aderenza sufficiente al Percorso Diagnostico Terapeutico Assistenziale (PDTA) proposto?
Risposta
AB si è presentato a tutti i controlli ambulatoriali programmati e ha riferito un progressivo miglioramento soggettivo (riduzione dei sintomi specifici di scompenso glicemico acuto a 3 giorni dall’inizio del trattamento e remissione dopo 8 giorni). I dubbi esposti dal paziente sono stati risolti durante le visite mediche (es. un’iniziale riduzione del visus dopo l’inizio della terapia intensiva motivata dalla progressiva riduzione dei valori glicemici si è risolta al T1).
3° step
Alla rivalutazione programmata a 12 mesi dalla diagnosi (T3) gli esami ematochimici evidenziavano: glicemia a digiuno di 108mg/ dl, HbA1c stabile (5,5%), microalbuminuria in norma; peso corporeo in moderato aumento (+2 kg da T2, -8 kg da T0). Buona aderenza alla terapia alimentare. Viene riconfermata la sola terapia alimentare, dimesso dal nostro SD e avviato al monitoraggio glicometabolico con il MMG secondo protocollo di Gestione Integrata.
Dopo 24 mesi (T4) di Gestione Integrata AB è stato inviato dal MMG al nostro SD per rivalutazione. Dal raccordo anamnestico che AB esibisce non si rileva nulla di nuovo in anamnesi patologica in questo intervallo di tempo; ha mantenuto la sola terapia diabetologicaalimentare. Ha eseguito recente controllo del fondo 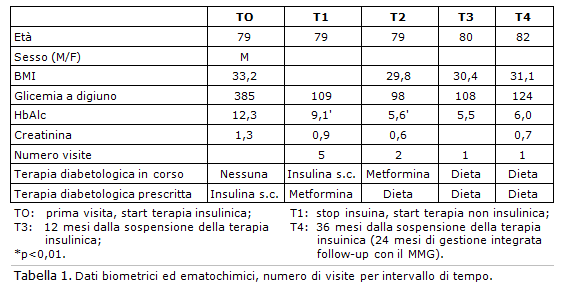 oculare senza evidenza di retinopatia diabetica; ha eseguito inoltre ECG e visita cardiologica con valutazione di buon compenso emodinamico e pressorio in cardiopatia ischemica nota, stabilizzata. Peso in lieve aumento (+2 kg). Gli esami ematochimici rilevano un compenso glicemico ancora adeguato (HbA1c 6,0%) con glicemia a digiuno di 124 mg/dl. Profilo lipidico, funzione renale ed epatica in norma.
oculare senza evidenza di retinopatia diabetica; ha eseguito inoltre ECG e visita cardiologica con valutazione di buon compenso emodinamico e pressorio in cardiopatia ischemica nota, stabilizzata. Peso in lieve aumento (+2 kg). Gli esami ematochimici rilevano un compenso glicemico ancora adeguato (HbA1c 6,0%) con glicemia a digiuno di 124 mg/dl. Profilo lipidico, funzione renale ed epatica in norma.
Al T4 è stato sottoposto a screening del piede (non rilevate alterazioni della sensibilità al monofilamento, non significative deformità né lesioni cutanee) e a rivalutazione dietistica. Confermata la terapia alimentare, AB è stato reinviato alla Gestione Integrata con il MMG.
Tutti i dati biometrici ed ematochimici principali e il numero di viste specialistiche diabetologiche effettuate per intervallo di tempo per il paziente AB sono riassunte in Tabella I.
Domanda
Perché dopo la visita al T3 non è stata programmata una successiva visita di controllo presso il nostro SD?
Risposta
Nella nostra ASL è in atto l’assistenza integrata alla persona con diabete mellito tipo 2 secondo il protocollo della “Gestione Integrata”.
Infatti, con l’accordo Stato-Regione del 23-03-2005 è stato approvato il Piano Nazionale di Prevenzione (PNP) 2005-2007 che ha focalizzato tra gli obiettivi prioritari: la prevenzione delle malattie cardiovascolari e la riduzione delle complicanze del diabete mellito.
Per il diabete mellito il PNP ha identificato il Progetto IGEA, come strumento di realizzazione capillare in ogni Regione e per ogni ASL, delle modalità di assistenza da erogare alle persone con diabete per raggiungere il risultato atteso. Nell’ambito di tale progetto è stato prodotto un documento di indirizzo dal titolo “Gestione Integrata del diabete mellito tipo 2”, contenente informazioni sulle modalità organizzative essenziali per la gestione integrata della malattia da parte del Team multidisciplinare di cura, in particolare della Medicina Generale e delle Strutture Specialistiche per l’assistenza alle persone affette da diabete mellito (SD).
Pertanto nel caso di AB, il nostro SD ha definito la diagnosi, effettuato un inquadramento terapeutico e l’Educazione Terapeutica e, infine, formulato un Piano di Cura personalizzato e condiviso con il MMG.
Il MMG ha poi effettuato una valutazione periodica del paziente secondo il Piano di Cura adottato, finalizzato al buon controllo metabolico e alla diagnosi precoce delle complicanze.
Commento
Nel periodo compreso tra l’inizio del 2006 e la fine del 2008 abbiamo valutato i dati di 44 pazienti (tra i quali AB) con DMT2 di nuova diagnosi in stato catabolico, trattati con terapia insulinica intensiva breve.
I nostri risultati hanno confermato che nel DMT2 di nuova diagnosi, in stato catabolico all’esordio, la terapia insulinica intensiva breve permette sia un efficace e rapido recupero dell’equilibrio glicemico sia la stabilizzazione del compenso nel medio-lungo periodo dopo la sospensione della terapia insulinica; i dati a 12 mesi evidenziano una stabilità del compenso, mantenuta senza significativi cambiamenti della strategia terapeutica impostata alla sospensione. Questi dati trovano conferma anche in un più recente studio effettuato su pazienti diabetici di tipo 2 di nuova diagnosi con iperglicemia severa (glicemia a digiuno > 300 mg/ dl o random > 400 mg/dl) trattati con terapia insulinica intensiva per 10-44 giorni 11.
La possibilità di trasferire la maggior parte dei pazienti, 43 su 44, a terapia non insulinica, avvalora le osservazioni che una rapida riduzione della glucotossicità migliora l’insulino-sensibilità e verosimilmente anche l’insulino-secrezione, riduce l’apoptosi betacellulare e pone le basi per un periodo prolungato di compenso adeguato 12.
L’adesione da parte dei pazienti verso tale approccio è stata positiva nella maggior parte dei casi. È possibile anzi che il trattamento domiciliare intensivo dell’iperglicemia favorisca la consapevolezza e la motivazione del paziente e migliori la partecipazione attiva all’autogestione globale della sua condizione.
Sono peraltro auspicabili studi di confronto con altre modalità di trattamento per la valutazione dei costi e dell’efficacia preventiva sui rischi di ricovero correlati allo stato catabolico all’esordio e sugli esiti di salute a lungo termine conseguenti alla riduzione del tempo di esposizione dell’organismo alla cronica iperglicemia e quindi al miglioramento della memoria metabolica.
Sono note altre strategie di trattamento dell’iperglicemia 13 in scompenso cronico. Sicuramente l’elemento determinante, al di là della scelta farmacologica raccomandata, è la tempestività dell’intervento che in generale presuppone una preparazione del paziente. Pochi studi hanno valutato l’approccio insulinico all’esordio; tale terapia prevede un alto coinvolgimento del paziente e del team e richiede competenze e pianificazione di interventi articolati e coerenti ai bisogni del paziente.
Secondo la nostra esperienza l’approccio insulinico intensivo è time- consuming ma “rende” in termini di migliore motivazione del paziente e in termini di riduzione del numero di accessi al followup. È possibile che questa dimensione operativa favorisca un più elevato grado di consapevolezza della malattia diabetica e delle opzioni terapeutiche, modifichi il livello di attenzione del paziente e il suo all’approccio generale allo stile di vita necessario che richiede una partecipazione quotidiana e che può essere molto redditizia in termini di esiti di salute personale e collettiva.
La registrazione di alcuni dati di attività può servire a diversificare il lavoro necessario per il miglioramento della qualità dell’assistenza e degli esiti di salute.
La riduzione del carico di visite necessarie per il follow-up del paziente tempestivamente stabilizzato evidenzia l’efficienza di un disegno assistenziale orientato a dare concretezza alle raccomandazioni in termini di obiettivi condivisi e risultati percepibili soprattutto dal paziente come risposta al suo impegno in un tempo definito.
La centralità del paziente e del suo bisogno di salute si declina nella risposta appropriata ai suoi bisogni per una partecipazione attiva alla gestione della sua condizione; ciò è realizzabile con una diabetologia organizzata per offrire attività/prestazioni coerenti con le evidenze e coniugati con le diversità delle persone.
Bibliografia
-
Nathan DM, Buse JB, Davidson MB, et al. Management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy: a consensus statement from The American Diabetes Association and The European Association for the Study of Diabetes. Diabetes Care 2006;29:1963-72.
-
R yan EA, Imes S, Wallace C. Short-term intensive insulin therapy in newly diagnosed type 2 diabetes. Diabetes Care 2004;27:1028-32.
-
Alvarsson M, Sundkvist G, Lager I, et al. Beneficial effects of insulin versus sulphonylurea on insulin secretion and metabolic control in recently diagnosed type 2 diabetic patients. Diabetes Care 2003;26:2231-7.
-
Li Y, Xu W, Liao Z, et al. Induction of long-term glycemic control in newly diagnosed type 2 diabetic patients is associated with improvement of beta-cell function. Diabetes Care 2004;27:2595-602.
-
Ceriello A. La “memoria metabolica”: la nuova sfida nella terapia del diabete. Il Diabete, 2008;20:205-14.
-
ADVANCE Collaborative Group, Patel A, MacMahon S, Chalmers J, et al. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes. N Engl J Med 2008;358:2560-72.
-
Holman RR, Paul SK, Bethel MA, et al. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med 2008;359:1577-89.
-
Peters Al, Davidson MB. Maximal dose glyburide therapy in markedly symptomatic patients with type 2 diabetes: a new use for an old friend. J Clin Endocrinol Metab 1996;81:2423-7.
-
Davidson MB. Early insulin therapy for type 2 diabetic patients: more cost than benefit. Diabetes Care 2005;28:222-4.
-
Kahn SE, Haffner SM, Heise MA, et al.; ADOPT Study Group. Glycemic durability of rosiglitazone, metformin or glyburide monotherapy. N Engl J Med 2006;355: 2427-43.
-
Harn-Shen C, Tzu-En W, Tjin-Shing J, et al. Beneficial effects of insulin on glycemic control and beta-cell function in Newly diagnosed type 2 diabetes with severe hyperglycemia after shortterm intensive insulin therapy. Diabetes Car 2008;31:1927- 32.
-
Wajchenberg BL. Beta-cell failure in diabetes and preservation by clinical treatment. Endocr Rew 2007;28:187-218.
-
Standl E, Schnell O. Insulin as a first-line therapy in type 2 diabetes. Should the use of sulfonylureas be halted? Diabetes Care 2008;31:S136-9.



